Mit dem Heizwert bzw. der Verbrennungsenergie befassen wir uns in diesem Artikel. Dazu werden auch entsprechende Formeln mit Beispiel vorgestellt. Dieser Artikel gehört zum Bereich Thermodynamik.
Wer möchte es schon gerne kalt haben im Winter? Wer nutzt - zumindest in Mitteleuropa - nicht gerne ein Auto als Fortbewegungsmittel für weite Strecken? In beiden Beispielen geht es um die Verbrennungswärme bzw. den Heizwert. Im Falle der Heizung für den kalten Winter ist es Absicht, dass Verbrennungswärme entsteht. Beim Auto hingegen ist die Wärme durch die Verbrennung von Benzin dagegen ein Problem, denn die durch Wärme "verloren" gegangene Energie kann nicht mehr in Bewegung umgesetzt werden. Man benötigt aus diesem Grund vergleichsweise viel Treibstoff um eine Strecke mit dem Auto zu bewältigen.
Sehen wir uns nun das Ganze etwas näher aus dem Blick der Physik an: Bei jeder Verbrennung entsteht Wärme. Das Verhältnis aus der bei der Verbrennung frei werdenden Wärme zur verbrannten Masse wird als Heizwert bezeichnet. Es gibt zwei Formeln in diesem Bereich, die man kennen sollte. Bei der ersten Formel geht es um die Berechnung der Verbrennungsenergie bzw. des Heizwertes für feste Stoffe. Die zweite Formel stellt den Zusammenhang für flüssige und gasförmige Stoffe her.
Feste Stoffe:
Die Formel für feste Stoffe stellt den Zusammenhang zwischen der Verbrennungswärme, dem Heizwert und der Masse dar.
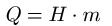
Dabei ist:
- "Q" die Verbrennungswärme in Megajoule [ MJ ]
- "H" der Heizwert in Megajoule pro Kilogramm [ MJ / kg ]
- "m" die Masse in Kilogramm [ kg ]
Flüssige / Gasförmige Stoffe:
Die Formel für flüssige und gasförmige Stoffe stellt den Zusammenhang zwischen der Verbrennungswärme, dem Heizwert und dem Volumen dar. Dies gilt für den so genannten Normalzustand ( Druck von 1013 mbar = 101,325 kPa und 0 Grad Celsius ).

Dabei ist:
- "Q" die Verbrennungswärme in Megajoule [ MJ ]
- "H'" der Heizwert in Megajoule pro Liter [ MJ / l ]
- "VN" das Volumen in Liter [ l ]
Beispiel:
Die Verbrennungswärme eines Motors soll berechnet werden. Verbrannt werden sollen 10l Benzin mit einem Heizwert von 37MJ/l.
Lösung: Wir entnehmen dem Text die Angaben und berechnen damit die Verbrennungswärme Q für 10l Benzin.

Links:
376 Gäste online
Anzeige:
Anzeige:
Verfügbare Fächer:
Anzeige:
Anzeige:
